研究摘要
软骨素是合成软骨素硫酸盐的关键前体,在生物医药领域具有广泛应用。传统微生物合成常面临胞内积聚、产量低等瓶颈。本研究以益生菌大肠杆菌Nissle 1917 (EcN)为底盘,通过系统重构软骨素合成模块、β-Kdo连接子通路及ABC转运系统,并结合聚合酶KfoC的理性设计,最终实现了软骨素的高效分泌生产。在5-L补料分批培养中,产量达到5.58 g/L,分泌效率高达92.3%。
EcN作为一种天然产生肝素前体(Heparosan)的益生菌,具备合成UDP-糖前体的代谢基础及基本的荚膜多糖转运机制 。研究人员通过CRISPR/Cpf1系统敲除内源肝素合成基因簇kfiABC,在此基础上构建了三个核心模块:模块I(软骨素合成通路优化)、模块II(β-Kdo连接子通路重构)以及模块III(ABC转运蛋白协同调控) 。
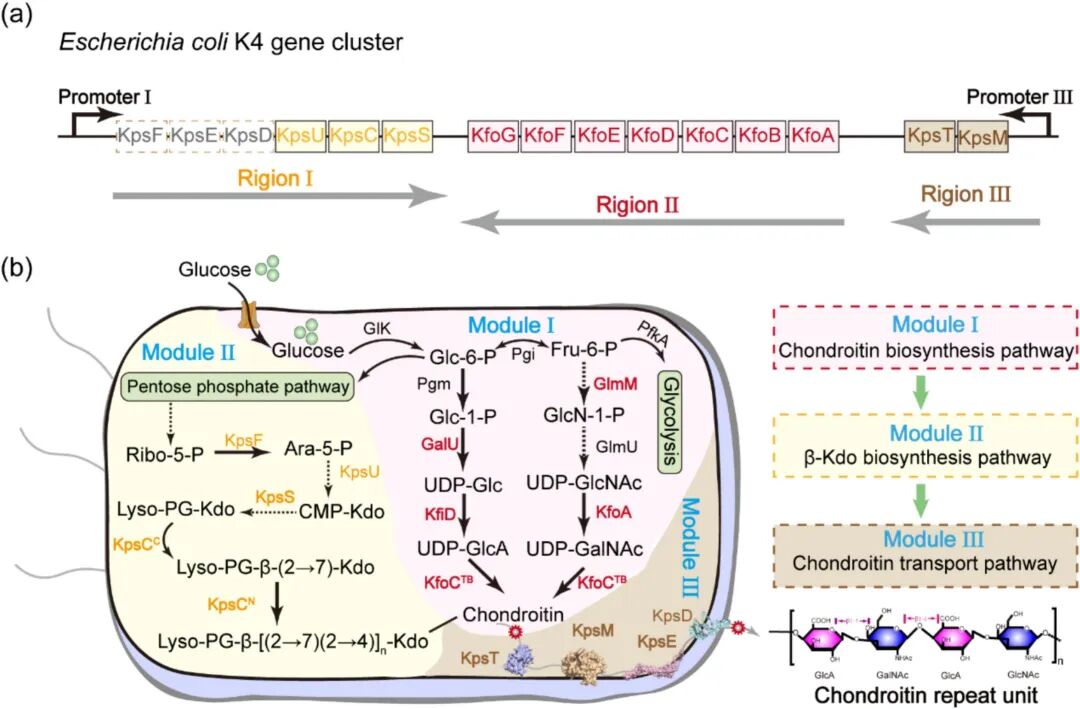
Figure 1. Chondroitin biosynthesis gene cluster and schematic diagram of chondroitin synthesis in engineered EcN.
研究初期,通过在EcN中表达软骨素合酶基因簇kfoCA,软骨素产量仅为0.13 g/L,且产物主要在胞内积聚 。当进一步通过强化前体供应通路(如过表达bsgalU-eckfiD-ecglmM)提升通量时,虽然胞内产量增至0.21 g/L,但细胞生长受到严重抑制,OD600显著下降 。透射电镜观察显示,大量的胞内积聚导致细胞形态畸变和膜结构损坏,这表明分泌瓶颈是提升产量的首要障碍 。
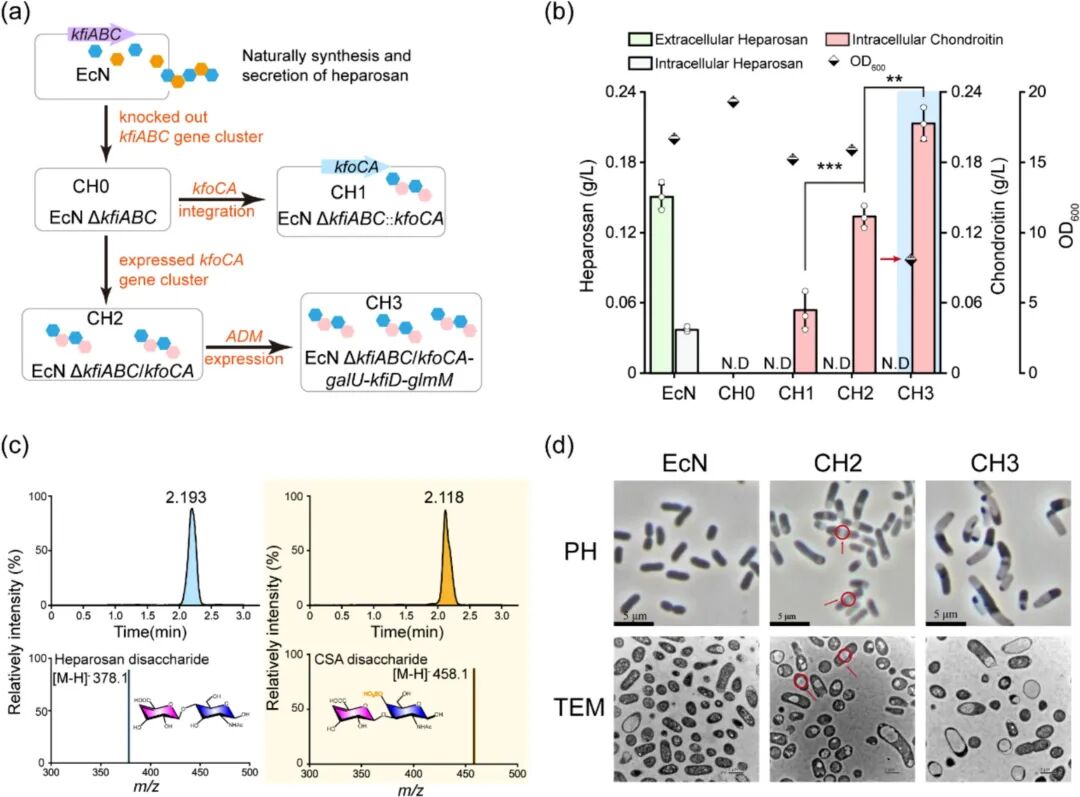
Figure 2. Development of engineered EcN strains for chondroitin synthesis.
通过比较基因组学分析发现,EcN内源的连接子通路无法有效识别并转运软骨素。研究引入了来自大肠杆菌K4的kpsC和kpsS基因,重构了β-Kdo连接子合成模块 。β-Kdo作为多糖链与脂质锚点之间的“桥梁”,其特异性对于多糖进入ABC转运通道至关重要 [1]。实验结果显示,协同表达KpsCK4和KpsSK4后,软骨素开始有效向胞外分泌,分泌率提升至57.14% 。
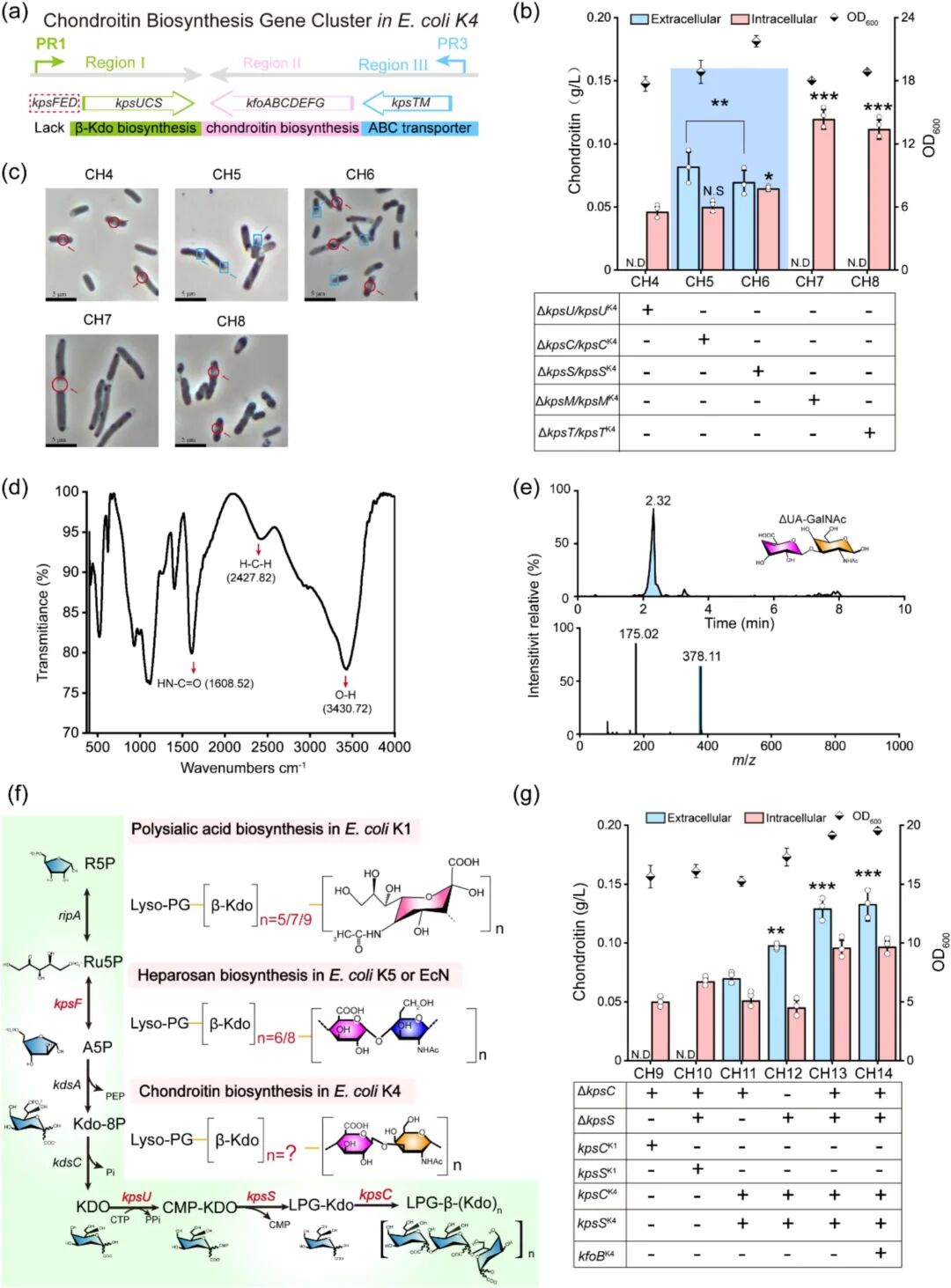
Figure 3. Eliminating the rate-limiting steps in the chondroitin secret.
为进一步加速跨膜转运,研究对ABC转运蛋白核心亚基(KpsT和KpsM)以及辅助转运蛋白(KpsE和KpsD)进行了系统优化。研究发现,协同过表达KpsTK4MK4并引入EcN内源的KpsE亚基,可使分泌率跃升至约72% 。KpsE可能参与形成了包围ABC转运蛋白的跨膜复合物,从而稳定了分泌通道 。
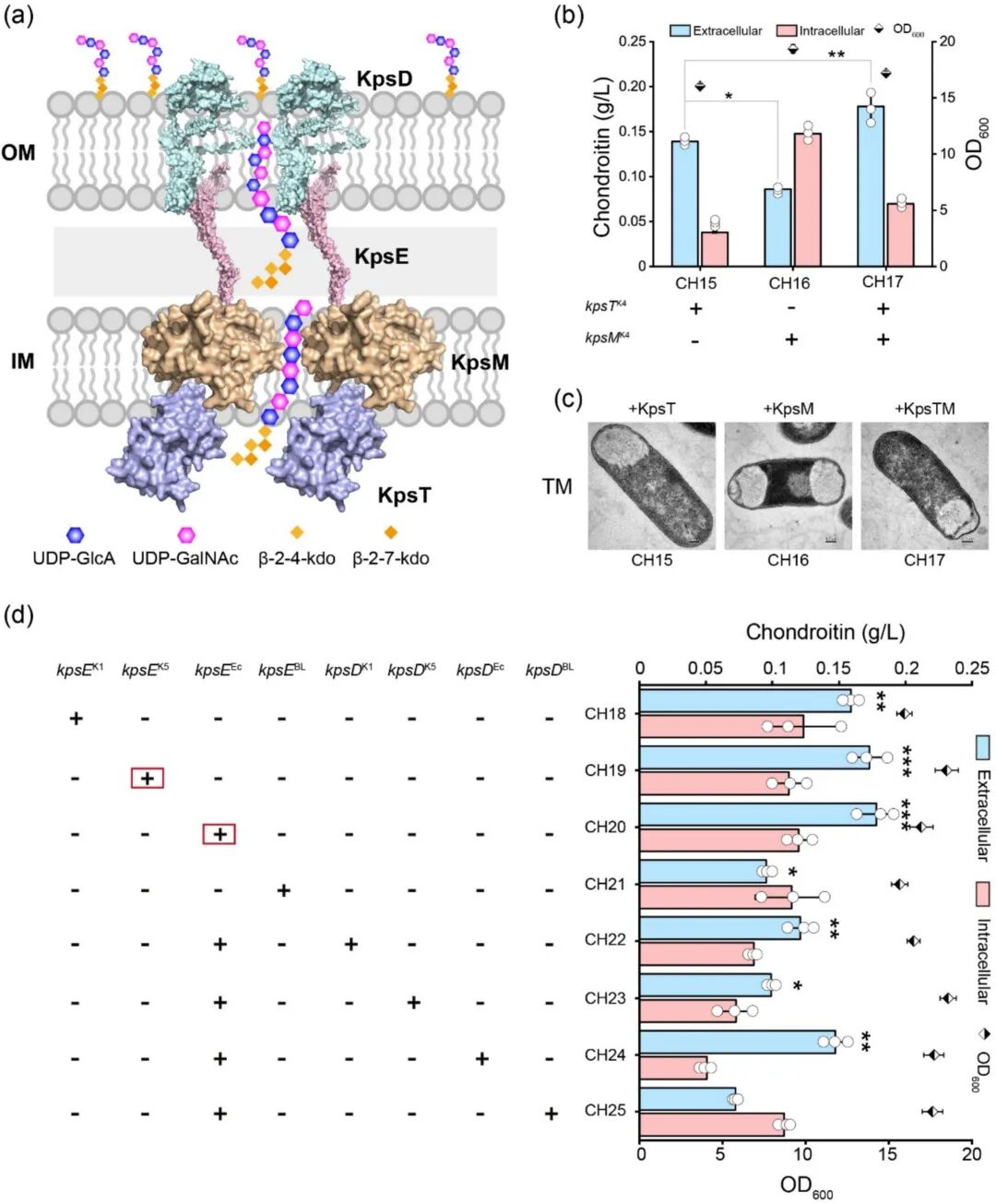
Figure 4. Coordinate the transport proteins with kfoCAB with kpsCS in the biosynthesis of chondroitin.
尽管分泌系统得到改善,但双功能聚合酶KfoC的催化效率仍是限速点。利用计算机辅助设计,研究人员针对KfoC非保守区域进行了柔性分析,并筛选出关键突变位点 。双突变体KfoC (T475S/H482Y)在摇瓶中将产量提升至0.44 g/L 。分子动力学模拟证实,这些突变减轻了催化口袋附近的位阻并稳定了活性中心结构 。
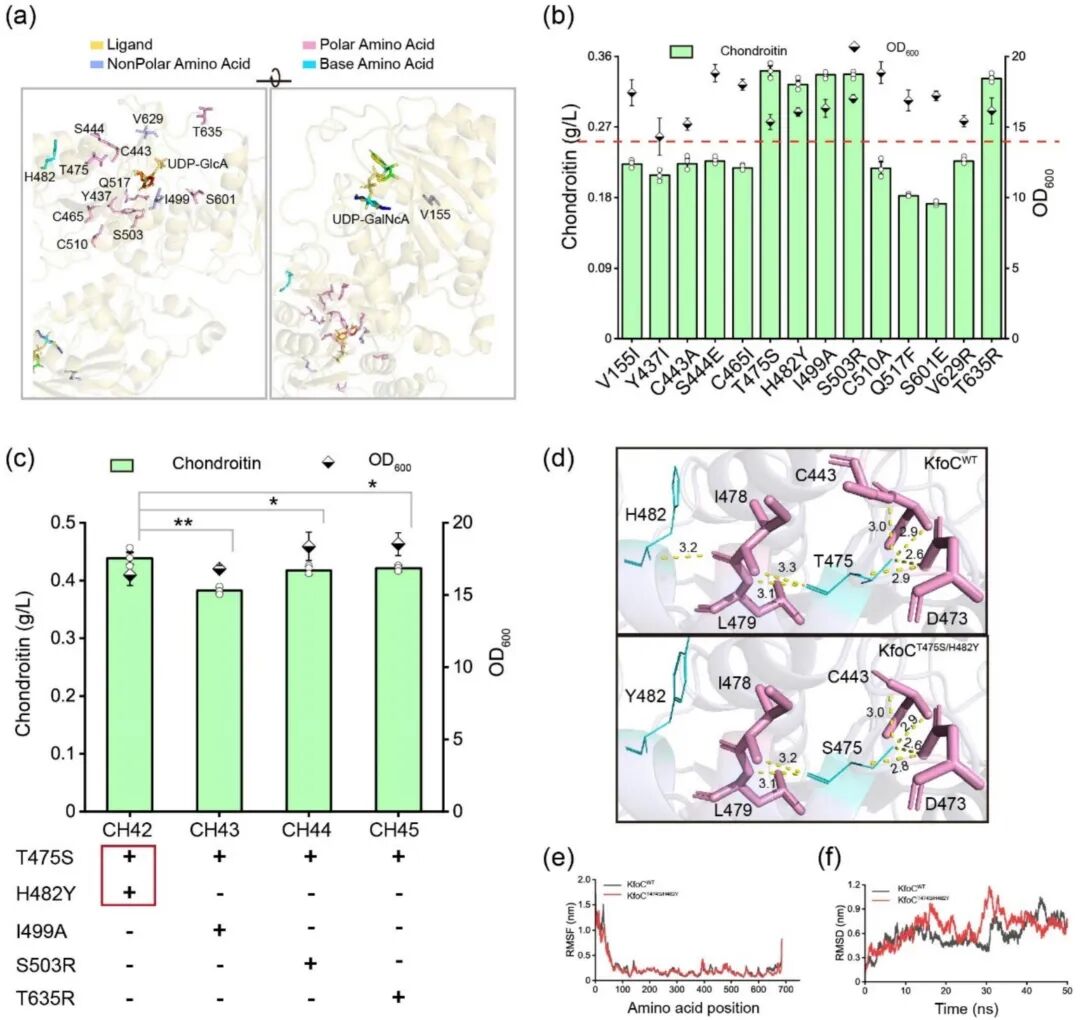
Figure 6. Structural and dynamic analysis of KfoC and its mutants.
最终工程菌株CH42在5-L发酵罐中表现出卓越的生产性能。通过指数补料策略,最大生物量OD600达到117.22 。发酵48小时后,总产量达到5.58 g/L,其中92.3%(约5.15 g/L)被分泌至胞外介质中,平均生产强度为42.8 mg/L/h 。HPLC-MS/MS分析证实,产物结构为典型的软骨素二糖重复单位 。
表 1. 菌株CH42在5-L发酵罐中的核心数据汇总
|
参数指标 |
数值 |
总软骨素产量 (g/L) |
5.58 |
分泌效率 (%) |
92.3 |
最大生物量 (OD600) |
117.22 |
生产强度 (mg/L/h) |
42.8 |
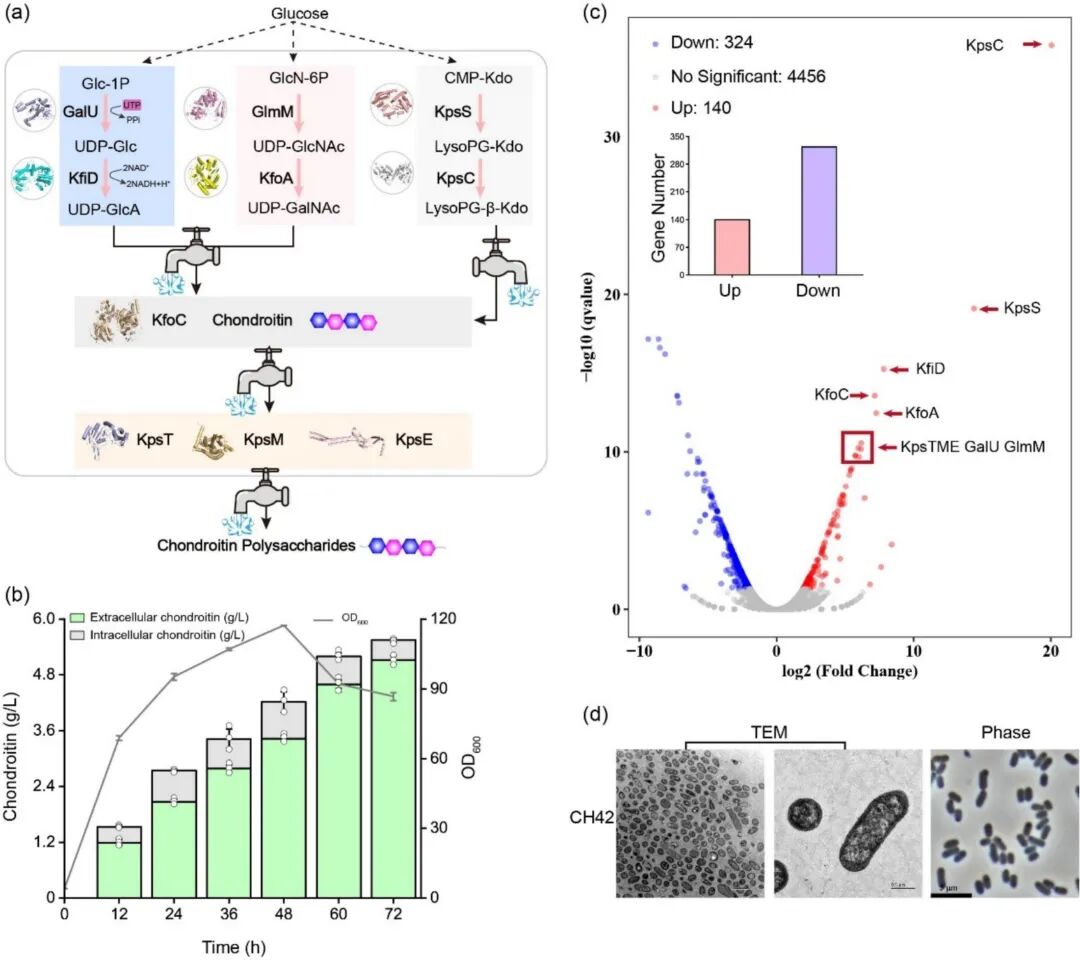
Figure 7. Fed-batch fermentation of engineered strain CH42 in a 5-L fermentation.
本研究通过重构β-Kdo通路和优化ABC转运系统,成功解决了异源多糖合成中的分泌难题。益生菌EcN作为一种高安全性的底盘,配合高效的分泌机制,为未来开发口服级软骨素及相关糖胺聚糖的微生物工厂奠定了坚实基础 。
