近日,Current Opinion in Biotechnology在线发表了江南大学糖化学与生物技术教育部重点实验室刘龙教授课题组的综述论文“Glycosyltransferases in human milk oligosaccharide synthesis: structural mechanisms and rational design” (Li et al., Current Opinion in Biotechnology. 2025. 93, 103315)。江南大学2024级博士后李阳阳为论文第一作者,刘龙教授为论文通讯作者。
母乳寡糖(HMOs)是母乳中的重要活性成分,具有调节婴儿肠道菌群、促进免疫系统发育及抑制病原体感染等多重生理功能。目前,已有180余种母乳寡糖结构被鉴定,其结构的多样性主要源于糖基化模式和糖苷键类型的差异,这与糖基转移酶的催化特性密切相关。然而,糖基转移酶普遍存在的催化效率低、底物特异性不足等问题,导致微生物合成母乳寡糖的产率较低。因此,研究糖基转移酶的结构特征与催化机制,并通过酶工程优化其性能,已成为提高母乳寡糖合成效率的关键。
为了促进糖基转移酶的理性设计及其在母乳寡糖合成中的应用,本文首先系统总结了目前已解析的糖基转移酶晶体结构,重点介绍了α-1,3-岩藻糖基转移酶(GT-B折叠)、β-1,4-半乳糖基转移酶(GT-A折叠)等关键酶的三维结构,并详细分析了它们保守的催化域特征和糖基转移反应机制;其次,概述了糖基转移酶的理性改造策略,包括通过删减跨膜结构域改善蛋白溶解性、重塑底物结合口袋提升催化效率、以及通过活性位点突变增强底物特异性等优化手段;最后,讨论并展望了人工智能驱动的蛋白质设计在糖基转移酶挖掘和改造中的应用潜力。
上述研究工作得到了国家重点研发项目(2023YFA0914500)、江苏省自然科学基金(BK20241619)、中国博士后科学基金会博士后创新人才支持计划(GZC20240610))及江苏省合成生物学基础研究中心项目(BK20233003)等项目的资助。
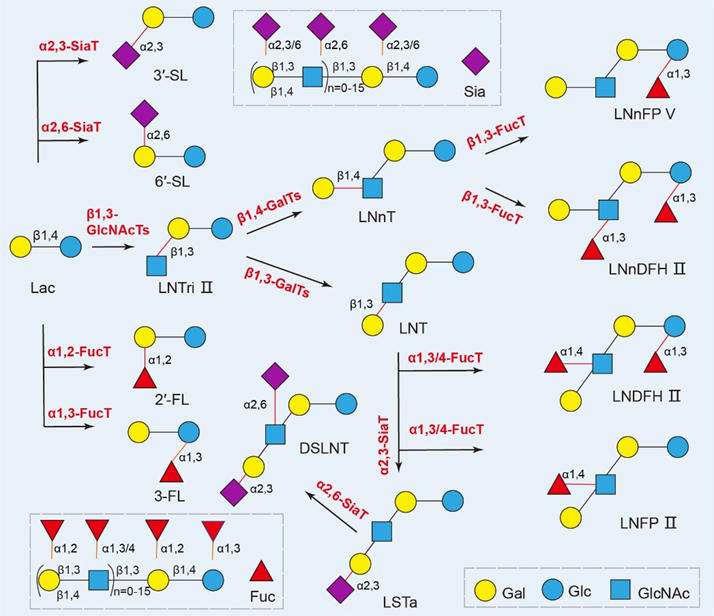
图1 糖基转移酶催化合成母乳寡糖示意图
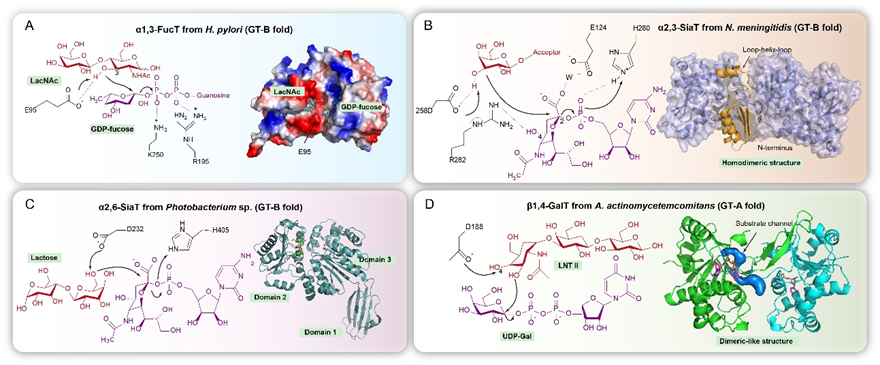
图2 合成母乳寡糖的糖基转移酶晶体结构及催化机制
