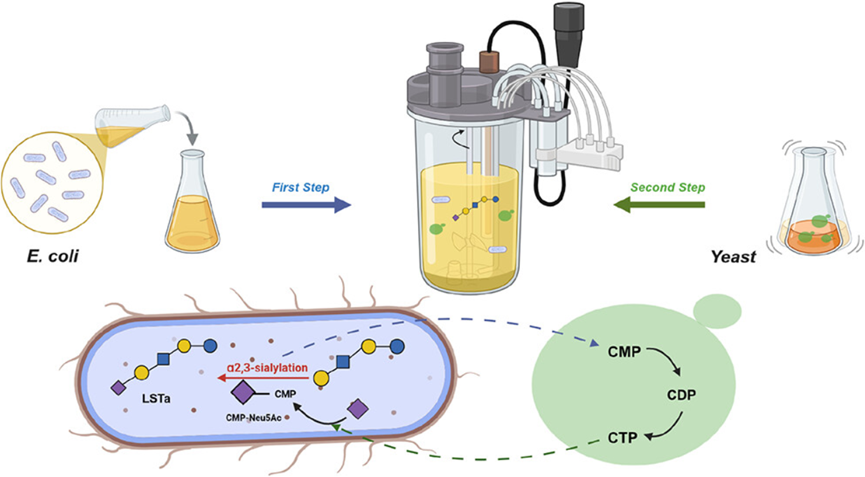
糖化学与生物技术教育部重点实验室张洪涛团队在《Journal of Agricultural and Food Chemistry》发表研究,构建大肠杆菌-酿酒酵母模块化细胞耦合全细胞催化体系,高效合成唾液酸化母乳低聚糖LSTa。经酶筛选、模块分工、条件优化与发酵放大,最终在5 L发酵罐实现LSTa产量38.03 g/L、底物转化率46.57%,为目前已报道最高水平,成功突破复杂唾液酸化HMOs合成中辅因子再生不足、催化效率低等关键瓶颈。
一、高效α-2,3-唾液酸转移酶筛选
研究以LSTa合成为目标,对脑膜炎奈瑟菌nst、空肠弯曲菌cstII、多杀巴斯德杆菌PmST1 M144D三种α-2,3-唾液酸转移酶进行异源表达与催化对比。结果显示,PmST1 M144D催化活性最高,底物转化率达22.77%,显著优于另外两种酶,确定为LSTa合成核心催化元件;同时选用空肠弯曲菌neuA编码的CMP-Neu5Ac合成酶,完成前体合成模块构建,为后续合成奠定酶学基础。
二、双菌株耦合体系与共表达优化
为解决CTP成本高、再生效率低的行业难题,团队设计模块化细胞分工耦合策略:大肠杆菌负责neuA与PmST1 M144D共表达,完成CMP-Neu5Ac合成与LSTa生成;酿酒酵母利用内源代谢实现CTP高效循环再生,持续供给高能辅因子。在此基础上优化表达载体,高拷贝质粒pRSFDuet-1介导的菌株E02表现最优,成功实现双模块高效协同,大幅提升反应可持续性与经济性。
三、全细胞催化条件系统优化
通过单因素实验系统优化诱导与催化关键参数:诱导条件确定为25℃、0.5 mM IPTG诱导20 h,保证蛋白可溶性高效表达;菌体配比为大肠杆菌25 g/L+酵母50 g/L(1:2),平衡催化与辅因子再生效率;底物比例Neu5Ac:LNT=2:1,避免底物抑制;催化条件为37℃、初始pH=8.0、反应30–35 h,产物积累达到峰值。优化后摇瓶产量达36.99 g/L,为规模化生产提供稳定工艺基础。
四、5 L发酵罐两步法放大验证
采用菌体培养诱导-全细胞催化两步法工艺放大生产:第一阶段37℃培养菌体至OD₆₀₀≈20,降温至25℃诱导目标蛋白表达;第二阶段加入酵母细胞与底物,调节pH至8.0,37℃进行全细胞催化转化。最终催化32 h,LSTa产量达38.03 g/L,LNT转化率46.57%,大幅超越现有文献报道水平,验证了该体系的工业化可行性。
五、核心创新点
§ 首创大肠杆菌-酵母模块化细胞耦合合成模式,实现催化模块与辅因子再生模块分工协作,突破单菌株代谢失衡瓶颈;
§ 筛选并应用高活性α-2,3-唾液酸转移酶PmST1 M144D,显著提升LSTa合成效率;
§ 采用全细胞催化简化工艺,无需酶纯化,条件温和、成本低、易规模化;
§ 创造LSTa生物合成产量新纪录,为复杂唾液酸化HMOs高效合成提供全新技术。