
核心亮点 江南大学团队利用“计算机理性设计+L-岩藻糖生物传感器介导的半理性筛选”双引擎策略,成功重塑α-1,2-岩藻糖基转移酶(BKHT),在底盘大肠杆菌中实现了母乳寡糖核心成分2'-岩藻糖基乳糖(2'-FL)高达124.25 g/L的从头合成,且全程“零”副产物,一举突破高纯度HMOs工业化量产的成本瓶颈!
背景介绍:为什么纯净的2'-FL如此难得?
2'-岩藻糖基乳糖(2'-FL)是人类母乳中含量最丰富的寡糖,具有调节肠道菌群、促进神经发育等无可替代的益生功能,目前已获得美国FDA的GRAS(一般认为安全)认证,是婴幼儿配方奶粉和高端功能性食品的“兵家必争之地”。然而,当前的合成生物学量产之路存在一个致命痛点:副产物分离成本极高。目前工业界常用的α-1,2-岩藻糖基转移酶(如来自幽门螺杆菌的FutC或大肠杆菌的WbgL)往往存在“催化不专一”的毛病。它们在合成2'-FL的同时,会进行杂乱的α-1,3-岩藻糖基化反应,生成结构极其相似的副产物二岩藻糖基乳糖(DFL)。要在下游纯化工艺中将2'-FL与DFL分离开来,需要耗费巨额的色谱分离成本。为了解决这一痛点,研究团队摒弃了传统的FutC,选择了一种具有严格区域选择性(绝对不产DFL)的BKHT酶。但这把“手术刀”虽然精准,却不够锋利(催化效率低)。如何让它既精准又高效?一场融合了计算结构生物学与高通量生物传感器的“爆改”由此拉开序幕。
核心技术深度解析:底盘改造与“五突变”神酶的诞生
本研究展现了教科书级别的蛋白工程与代谢通路协同优化的底层逻辑。
1.慧眼识珠:锁定“零副产物”的催化核心 如图1A和1B所示,研究人员首先通过多序列比对和摇瓶发酵验证,对比了多种糖基转移酶。经典的FutC菌株在积累2'-FL的同时产生了大量DFL副产物;而表达BKHT的菌株(BI-BKHT)虽然摇瓶初始产量仅为18.4 g/L,但HPLC检测显示全程无DFL生成。这为后续的定向进化提供了一个绝对干净的遗传底盘。 (注:研究中使用的宿主细胞BWLAI已经是经过深度代谢网络重排的大肠杆菌,敲除了ΔnudD、ΔlacZ、ΔwcaJ等多个竞争通路基因,专为富集GDP-L-岩藻糖前体而生)
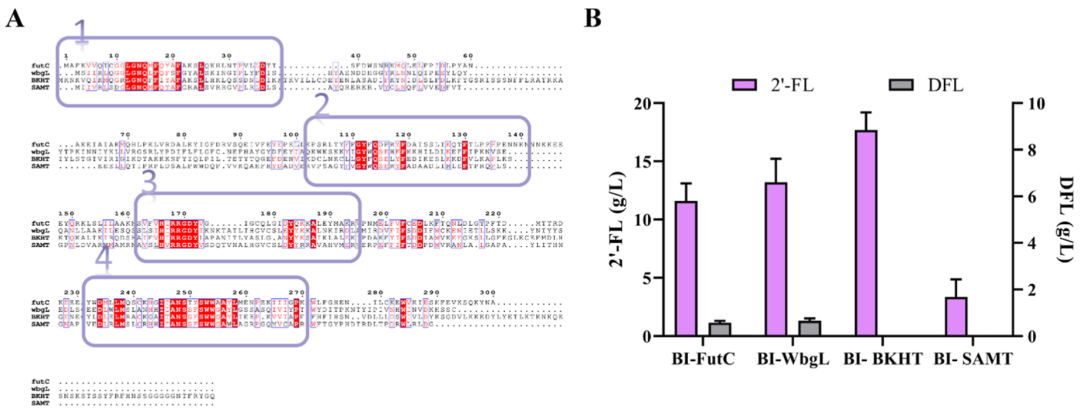
Figure 1. Comparison of α-1,2-fucosyltransferase yields based on literature reports
2.破局利器:构建并调优L-岩藻糖生物传感器 为了从海量突变库中快速捞取高活性突变体,传统HPLC检测显然太慢。研究团队巧妙利用细胞外的2'-FL水解产生L-岩藻糖的机制,构建了基于FcsR-PfcsK调控子的荧光生物传感器。 更精彩的是其基因线路调优(如图3B所示):初版传感器使用强T7启动子,导致FcsR表达过量,本底泄露严重(即没产物也亮)。研究团队通过将T7替换为可精密调控的PBAD启动子,并将其克隆至低拷贝质粒(pCS101 origin)上,极大地降低了基因表达负担和转录噪音。优化后的传感器在L-岩藻糖浓度与荧光信号之间展现出完美的线性关系,为高通量筛选(HTS)装上了“倍星镜”。
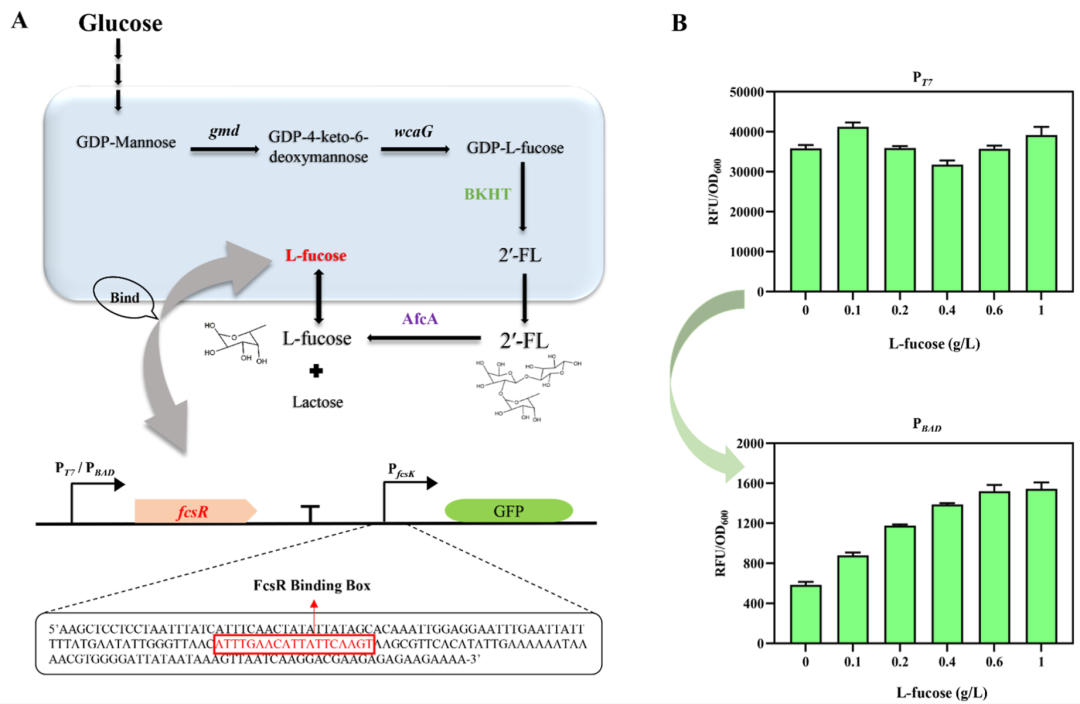
Figure 3
3.双剑合璧:理性设计结合半理性筛选 理性计算设计(图2):利用HotSpot Wizard预测活性口袋关键位点,PROSS算法预测提高蛋白稳定性的突变。摇瓶验证发现,稳定化突变L36P使产量提升21.5%(达24.9 g/L),而S317D提升了16.1%。
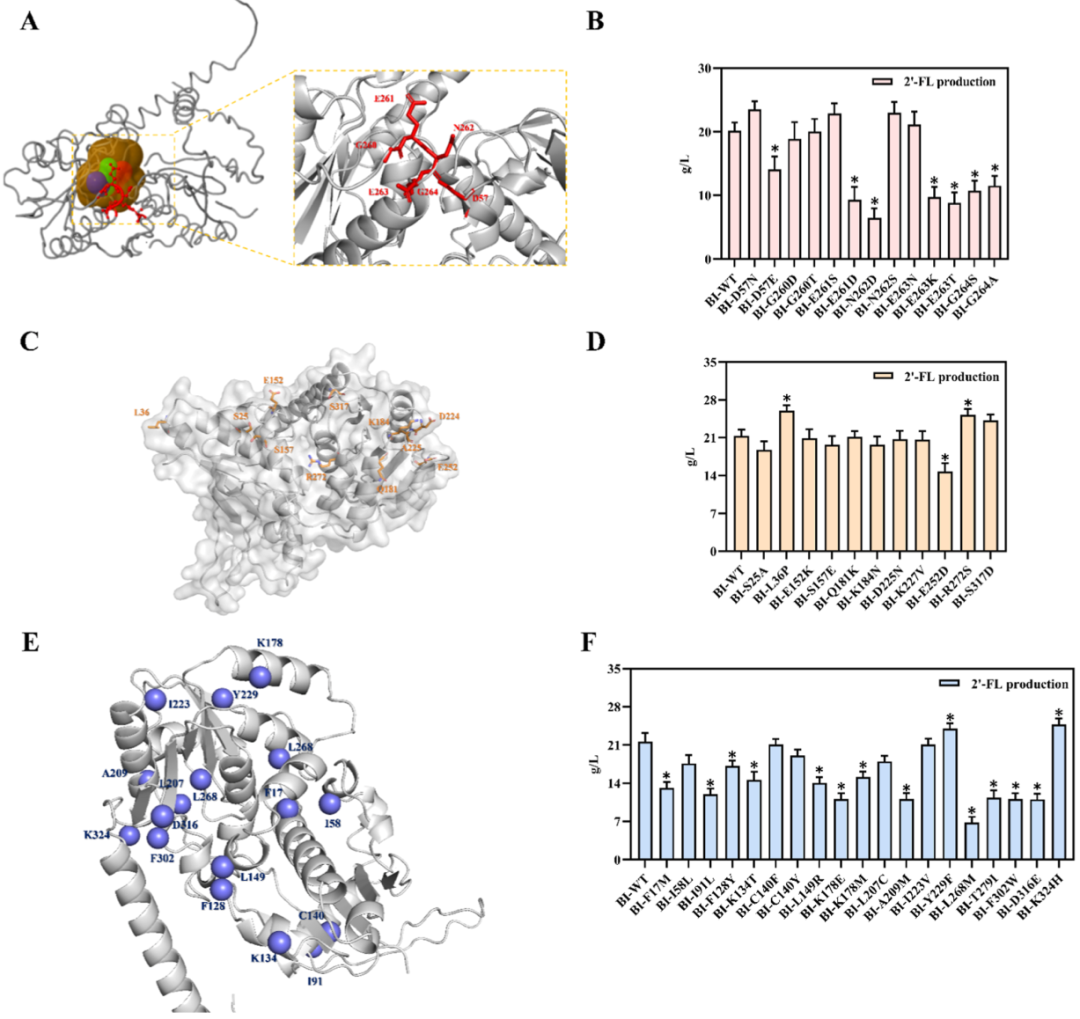
Figure 2
传感器引导的半理性筛选(图4):利用优化好的生物传感器,对ConSurf预测的非保守区(Motif 1-3)进行饱和突变库筛选。成功捞取了I58V(25 g/L)和E261G(25.5 g/L)两个极其关键的底物结合口袋突变。
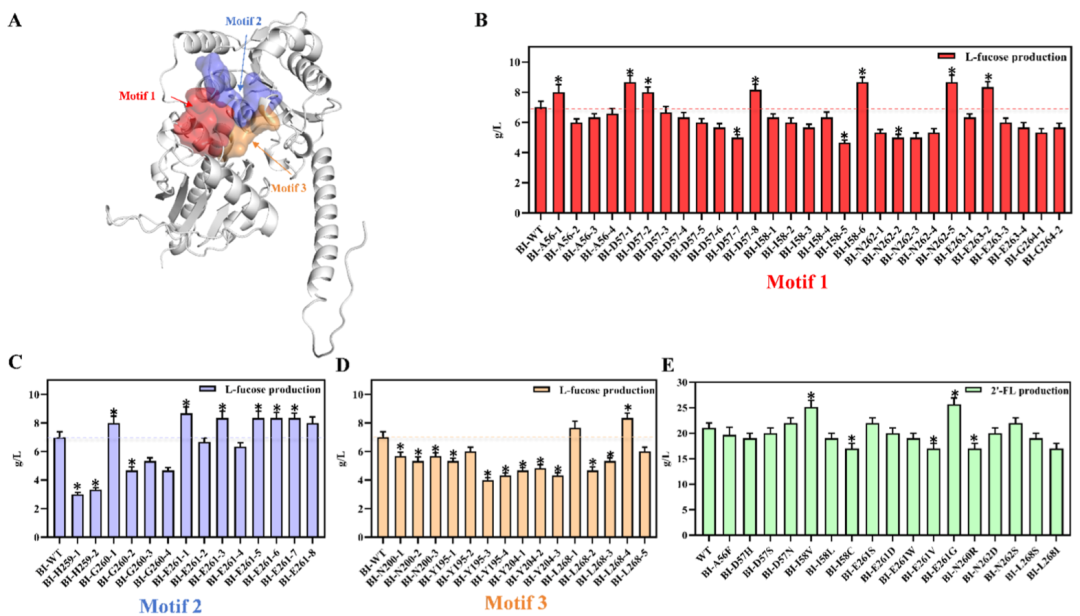
Figure 4
4. 终极进化与分子机制:M5组合突变体的诞生 研究者并没有止步于单点突变,而是进行了迭代组合组装(图5)。通过多轮堆叠,最终铸造出五重突变体M5(L36P−I58V−E261G−S317D−K324H),摇瓶产量飙升至32.1 g/L,较野生型提升了56.58%。
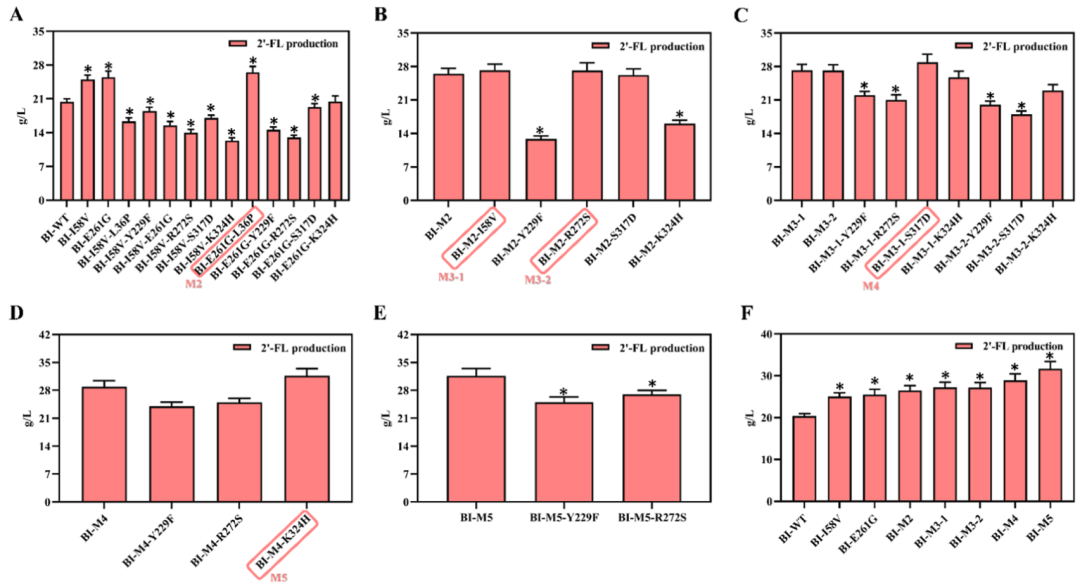
Figure 5. Combinatorial engineering of BKHT by integrating rationally and nonrationally identified mutations and evaluation of 2′-FL production in the production strain
为什么M5这么强?图6的分子动力学(MD)模拟和RMSF数据给出了底层解释:E261G突变将柔性Loop区(残基255-265)的柔性降低了约40%,将无序运动转化为有利于底物包裹的有序动态。L36P像一颗钢钉,刚性化了N端支架,减少了非功能性全局震动。MD计算表明,野生型酶与GDP-L-岩藻糖的结合自由能为-37.71 kcal/mol,而M5突变体显著下降至-48.12 kcal/mol。这种基于静电网络和构象稳定性的全面优化,是从底层逻辑上提升催化效率的终极密码。
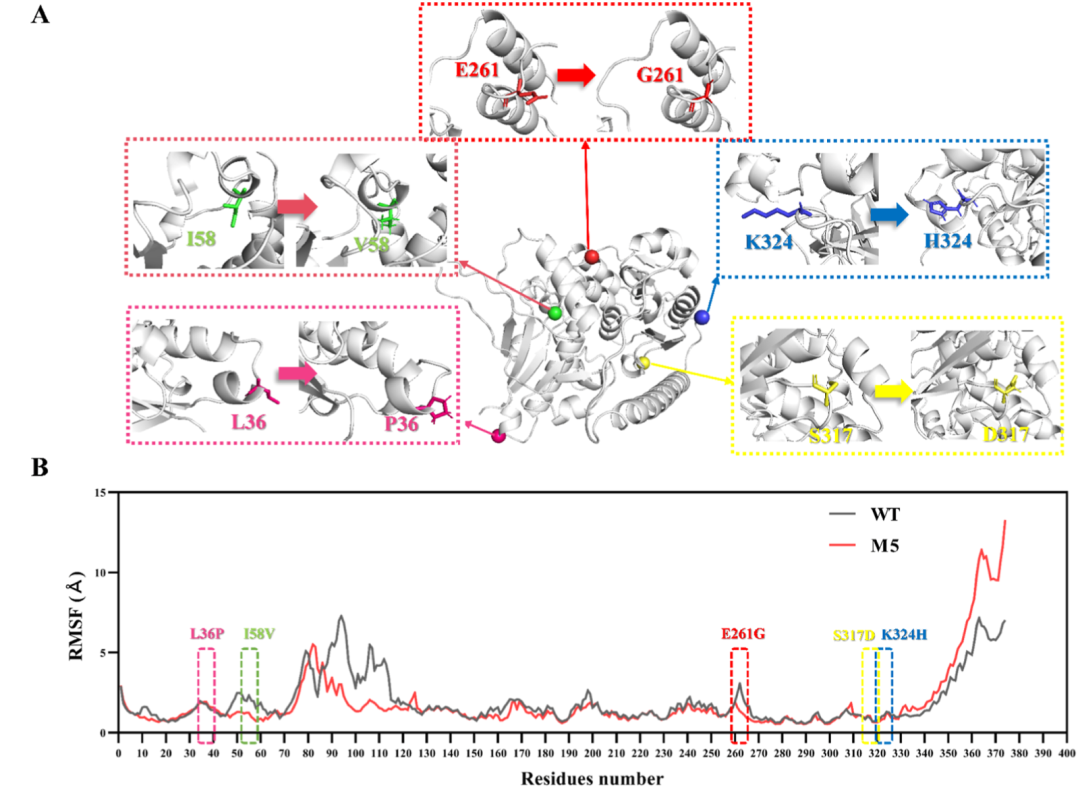
Figure 6. Structural analysis of the optimized mutant M5
产业化前景与商业价值评估
· 破纪录的发酵指标(结合图7):在3L反应器中,采用最廉价的葡萄糖作为唯一碳源,97.5小时内实现了124.25 g/L的2'-FL超高滴度合成。这一数据刷新了以葡萄糖为底物的国际最高纪录。其发酵周期短、时空产率高,直接摊薄了单批次设备的折旧成本。
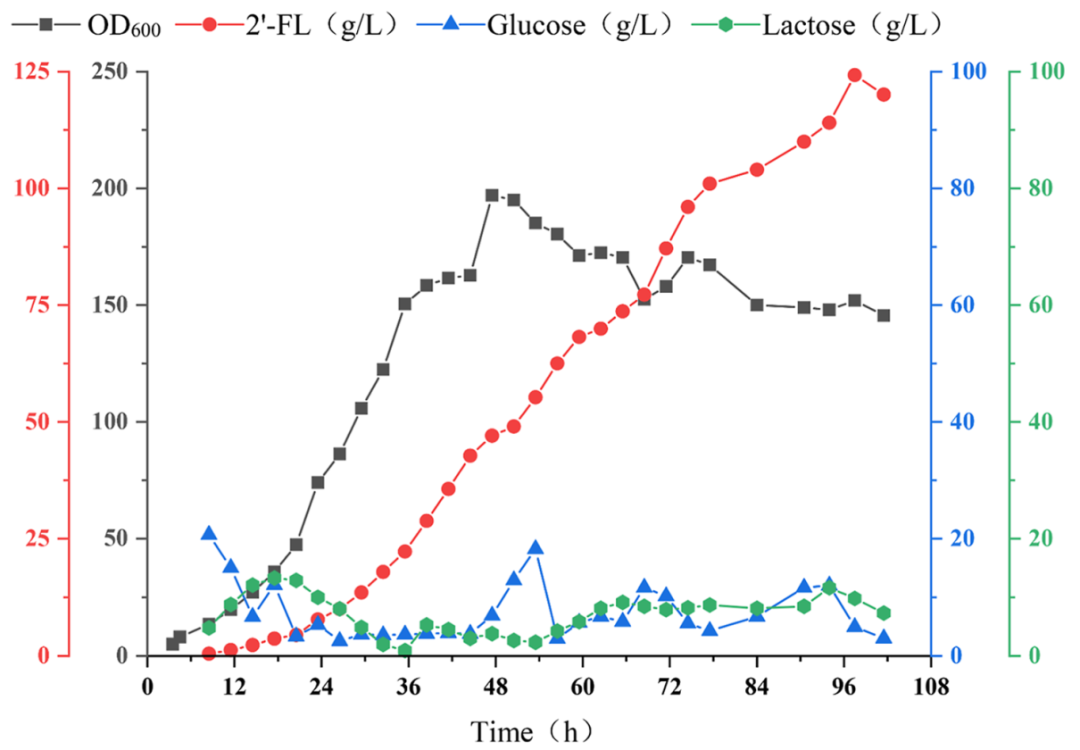
Figure 7. Fed-batch fermentation performance of the engineered strain BI-M5 (expressing the optimized BKHT mutant) in a 3 L bioreactor
· 极简的下游纯化(DSP):图7及全篇数据反复证实,即使在124 g/L的极高浓度下,依然“无检测限以上(no detectable)”的DFL副产物。对于寡糖产业而言,分离两个分子量相近的寡糖(2'-FL和DFL)极其依赖昂贵的模拟移动床(SMB)色谱。BKHT-M5的“零副产物”特性能让企业直接跳过或大幅简化色谱精制步骤,下游纯化成本有望断崖式下降30%-50%。
· 巨大的市场纵深:2'-FL不仅是配方奶粉的标配,其在成人肠道微生态调节、抗病原体粘附方面的药用/保健潜力正在被释放。使用该菌株平台,具备极强的商业护城河。
局限性与未来展望
尽管该研究展现了极高的工业转化潜力,但站在产业化前沿,仍有几个值得探索的优化方向:
· 大生产抗逆性验证:3 L反应器数据极其惊艳,但放大至10吨、100吨级别时,大肠杆菌底盘将面临更加复杂的溶氧不均、剪切力以及静水压问题。菌种在长时间连续传代和高压环境下的遗传稳定性,需进一步在先导工厂(Pilot Plant)进行压力测试。
· “去抗性标记”与食品级安全合规:本研究在质粒维持和传感器构建中仍使用了抗生素和诱导剂(IPTG/阿拉伯糖)。面向食品和婴配粉级应用,未来必须将这套完美的M5基因及其启动子整合至大肠杆菌染色体上,实现无抗生素发酵与自诱导/廉价诱导(如温度诱导),以彻底扫除法规与安全隐患。
· 平台技术的延伸:本研究中开发的低噪音“L-岩藻糖生物传感器”,不仅可以用于2'-FL,还可以作为一个通用插件,反向应用于其他含岩藻糖化合物(如3-FL或L-岩藻糖本身)的微生物细胞工厂改造,具备衍生出一系列管线产品的潜力。
