近期,江南大学生物工程学院、糖化学与生物技术教育部重点实验室尹健教授团队在细菌糖蛋白疫苗研究方面取得新进展,研究成果“Preclinical development of a well-defined semisynthetic glycoconjugate vaccine against Haemophilus influenzae type b”发表于Science Advances。

尹健教授团队长期专注“生物医药化工与糖疫苗工程”领域研究,系统研究并取得了一系列原创性成果,聚焦糖基化过程强化以及糖链的工业化制备、(耐药)细菌表面糖链抗原多样化结构库的构建、创新发展基于糖芯片的高通量筛选技术,以及候选糖蛋白疫苗系统性的临床前评价等,贯通“糖链高效获取——糖链表位挖掘——候选疫苗临床前评价”的细菌糖蛋白疫苗的全链条创新研究平台。
b型流感嗜血杆菌(Haemophilus influenzae type b,简称Hib)是引起细菌性呼吸道感染的常见致病菌,可导致儿童肺炎和脑膜炎等。荚膜多糖是Hib细胞表面的主要组分,全球已上市的Hib疫苗均采用该结构特异性聚核糖基核糖醇磷酸酯(polyribosyl-ribitol-phosphate, PRP)作为抗原。Hib糖疫苗的广泛应用使Hib相关疾病的发生率和死亡数均降低了90%以上。已上市Hib糖疫苗主要采用生物发酵提取多糖作为抗原结构,存在表位易缺失、污染物混入、质控精度低等长期困扰的问题。本世纪初,古巴上市了合成寡糖蛋白疫苗Quimi-Hib®,但所用糖链抗原为非定向合成的寡糖混合物,仍存在组分非均一、表位未明晰、质控精度低等不足,限制了其在全球范围的推广应用。针对现状,本研究聚焦Hib糖蛋白疫苗的迭代升级,系统性开展了基于均一合成寡糖的新一代Hib糖蛋白疫苗的临床前研究工作,包括:1)Hib荚膜多糖的高效定向制备,2)Hib荚膜多糖的免疫表位解析,3)候选Hib糖蛋白疫苗的临床前评价。
Hib荚膜多糖高效定向制备面临的核心难点为PRP特有磷酸二酯键的高效构建。为实现规模化的糖链制备,研究团队基于亚磷酰胺合成策略,设计并开发了PRP模块化组装技术,以单聚体和二聚体糖苷亚磷酰胺作为合成模块,实现了一至十二聚体的定向化和规模化制备;并解决了三苯甲基醚脱除不完全的技术难点,开发了三氟化硼乙醚/甲醇/二氯甲烷脱保护工艺,为新一代Hib糖蛋白疫苗的创制奠定了基础(图1)。
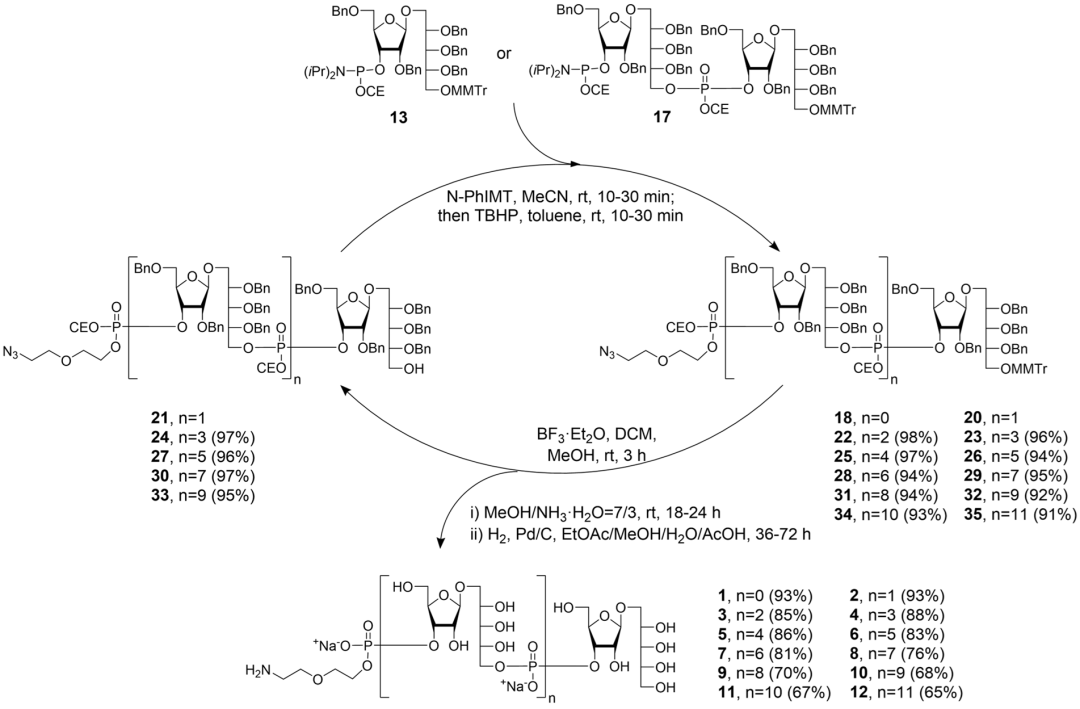
▲ 图1. 1-12聚PRP寡糖的模块化合成
为筛选最佳糖链抗原,研究人员发展糖芯片技术对合成PRP糖链进行了抗原性评估,发现2、4、6、11、12聚体糖链具有一定抗原性;进一步选取4、6、8、11、12聚体与TT载体结合(图2)。动物免疫实验结果显示各糖蛋白的缀合物均能诱导特异性抗体,其中4-TT糖缀合物诱导产生的IgG抗体滴度最高。糖芯片识别谱、荧光成像、流式与血清杀菌实验的交叉验证进一步证实4-TT诱导的抗体对Hib菌体具有最强结合亲和力与特异性杀菌活性,揭示了四聚体4为Hib荚膜多糖的关键免疫表位,是新一代Hib糖蛋白疫苗的优选抗原。
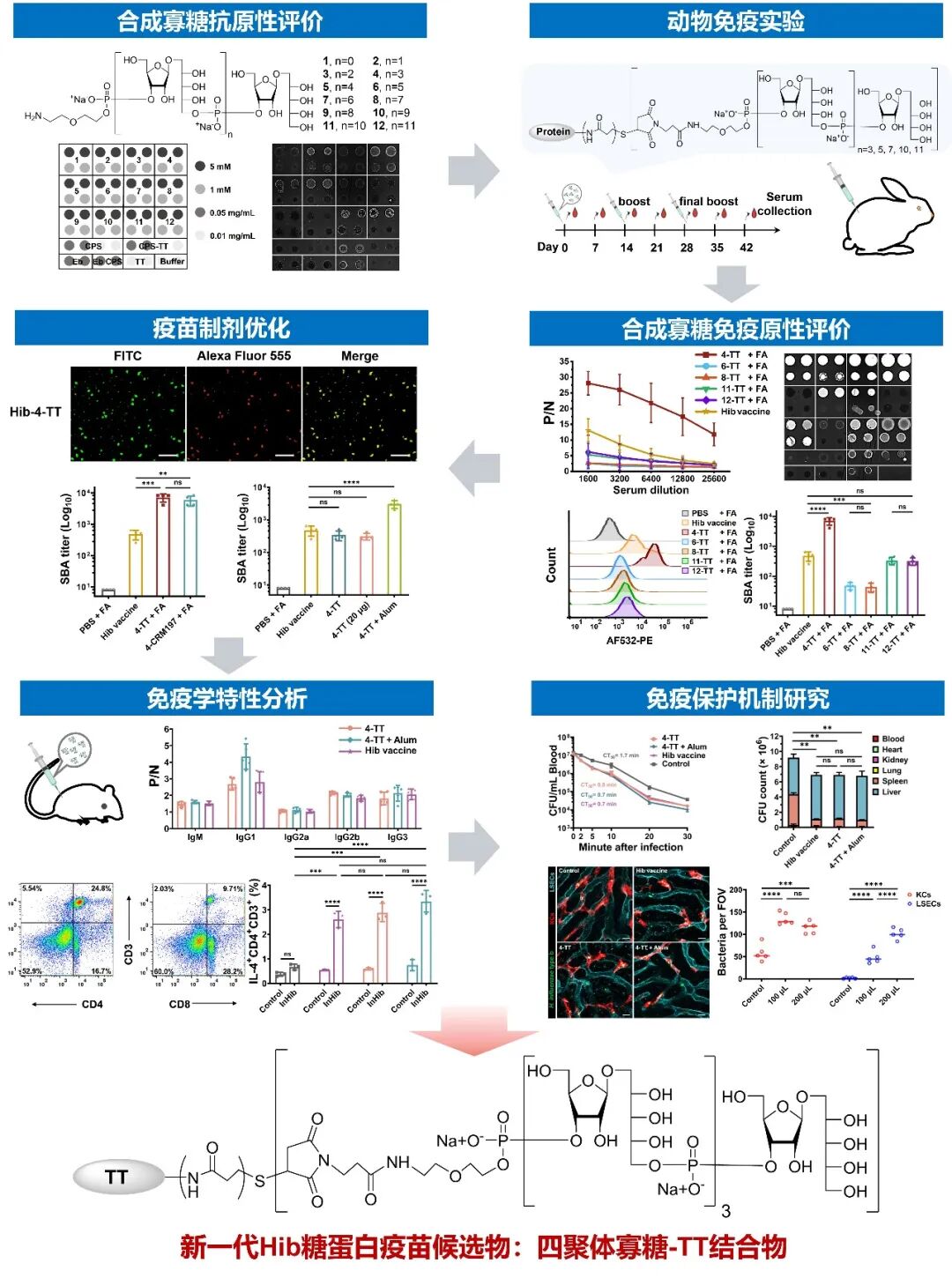
▲ 图2. 新一代Hib糖蛋白疫苗候选物的研究
在此基础上,研究团队以“疫苗制剂优化——免疫学特征解析——保护机制阐明”为主线,搭建了贯穿体内外的系统性评价平台(图2)。在疫苗制剂优化方面,四聚体与载体蛋白TT的缀合物在诱导IgG抗体滴度、菌体亲和力及血清杀菌活性方面均显著优于与CRM197的缀合物;在无佐剂条件下,四聚体缀合物4-TT在相同接种剂量下可获得与上市Hib多糖蛋白疫苗相当的免疫保护效力,而引入铝佐剂则显著加速了免疫启动,为快速建立免疫屏障提供了强效方案。进一步的疫苗免疫原性评价结果显示,无佐剂的4-TT不仅诱导了与上市疫苗同等水平的IgM及IgG全亚类应答,实现了高效的抗体类别转换,还显著上调了小鼠脾脏CD4+与CD8+ T细胞比例。此外,经灭活Hib菌体特异性刺激后,CD4+ T细胞中IL-4与IFN-γ的高表达进一步证实其能有效驱动Th1/Th2混合型细胞免疫应答。对疫苗保护机制研究也开展了研究,利用小鼠菌血症模型验证了4-TT抗血清突出的体内细菌清除能力,不仅能在30分钟内高效清除血液循环中的Hib致病菌,更通过抗体介导机制显著增强了肝脏驻留巨噬细胞(KCs)与肝窦内皮细胞(LSECs)对病原体的靶向捕获效率。上述系统性的研究确证了4-TT候选疫苗具备媲美现有商业疫苗的免疫保护效力,为其后续临床研究提供了详实、扎实的基础。
综上,研究团队在Hib荚膜多糖的糖链定向化和规模化制备基础上,精准锁定四聚体4这一关键免疫表位,创制的Hib糖蛋白疫苗候选物具有免疫保护效力突出、生产工艺稳定,糖链组分均一、表位清晰完整、质控精度高等诸多优势。上述临床前研究结果为推进后续临床试验提供了坚实而充分的科学支撑,也为细菌糖蛋白疫苗研发由“传统天然产物提取与经验导向的制剂开发”向“结构明确均一且可迭代的分子工程化设计”的跨越提供了具有范式意义的启示。
生物工程学院尹健教授和无锡医学院胡静教授为该论文的共同通讯作者,我校生物工程学院2021级博士研究生韩玮为论文第一作者,生物工程学院青年教师秦春君副研究员为论文共同第一作者。清华大学医学院张敬仁教授团队和北京民海生物科技有限公司为本研究提供了重要的支持。上述研究得到了国家自然科学基金(22325803, 22277042, 22478153, 22177041)和国家重点研发计划(2023YFC2308004)的资助。研究团队特别感谢江南大学分析测试与实验动物中心顾小红老师、江南大学生物工程学院分析测试平台雷洁和张琳培老师对本研究的帮助。
尹健,江南大学生物工程学院教授、博士生导师、院长,国家杰出青年科学基金获得者,糖化学与生物技术教育部重点实验室主任,糖疫苗与糖药物江苏省高校重点实验室主任,中国疫苗行业协会糖疫苗专业委员会副主任委员兼秘书长。长期专注“生物医药化工与糖疫苗工程”领域研究:(1)(耐药)细菌表面糖链的糖基化过程强化与规模化制备;(2)(耐药)细菌糖蛋白疫苗的迭代(b型流感嗜血杆菌、肺炎链球菌、脑膜炎奈瑟菌等)与创制(幽门螺旋杆菌、铜绿假单胞菌、肺炎克雷伯菌等);(3)高附加值糖类营养物质的生物制造。
