
亚甲基二氧桥环是一类非常重要的结构单元,广泛存在于低等植物、海洋动物、真菌等来源的天然产物和药物分子中,并且这类化合物具有抗菌、抗病毒、抗癌等多种生物活性。到目前为止,研究者们挖掘并证明了CYP719A、CYP81Q、Hkm5、StvP2等P450酶可以催化五元、六元亚甲基二氧桥环的形成,但是对于独特的七元亚甲基二氧桥环的形成机制仍不明确。尾孢菌素(cercosporin)是一种含有七元亚甲基二氧桥环的苝醌类色素,具有多种生物和光催化活性。尽管它已被分离和鉴定了几十年,但其生物合成途径,特别是独特的七元亚甲基二氧桥环的形成机制尚未研究。近日,饶义剑教授团队通过体外重构、晶体结构解析、定点突变和量子化学计算等手段阐明了尾孢菌素生物合成中七元亚甲基二氧桥环的形成机制,为解析其它含有亚甲基二氧桥环天然产物的生物合成途径提供了分子基础。
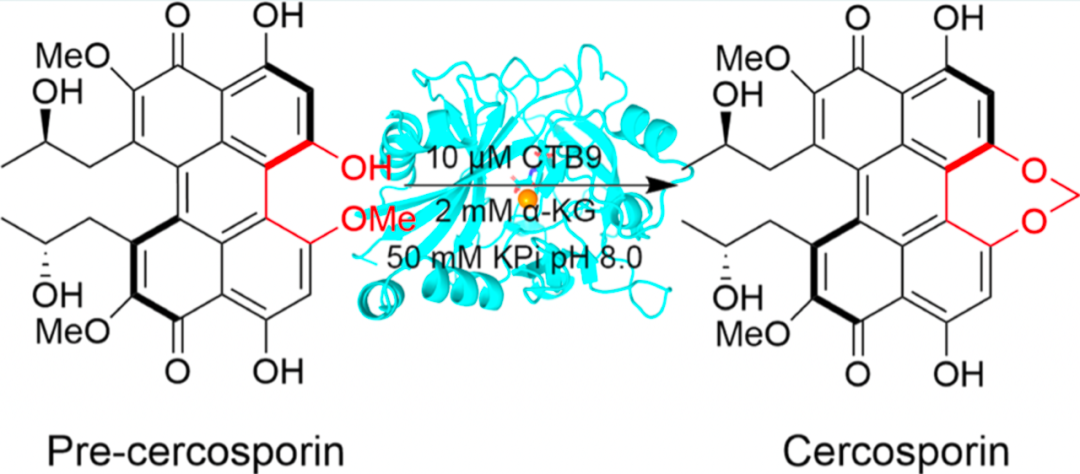
天然产物尾孢菌素的生物合成是由CTB基因簇编码的蛋白来完成(Fig. 1)。结合前期的研究基础(Zhou, et al, 2021, Microb Cell Fact;Li, et al, 2019, Green Chem; Wu, et al, 2021, J Hazard Mater;Wu, et al, 2021, Chem Eng J),首先,作者分别进行了基因敲除和体外细胞裂解液实验,实验结果表明在尾孢菌素的生物合成过程中只需要Fe(II)/α-KG依赖加氧酶CTB9就能催化七元亚甲基二氧桥环的形成(Fig. 2),而不需要CTB10的参与。
为了更好地理解CTB9的催化机理,作者解析了CTB9在催化过程中三种不同状态的晶体结构CTB9 (2.29 Å)、CTB9•Cu•NOG (2.49 Å)、CTB9•Cu•NOG•pre-cercosporin (2.20 Å) (Fig. 3)。通过比较不同状态下周围氨基酸构象的变化,可以清晰地观察到底物pre-cercosporin与周围氨基酸的相互作用。为了验证CTB9与底物pre-cercosporin的结合方式,作者进行了氨基酸保守性分析和基于晶体结构的定点突变,证实了这些位点的氨基酸残基在CTB9催化过程中起着关键作用,从而为阐明CTB9的催化机理提供了坚实的基础。
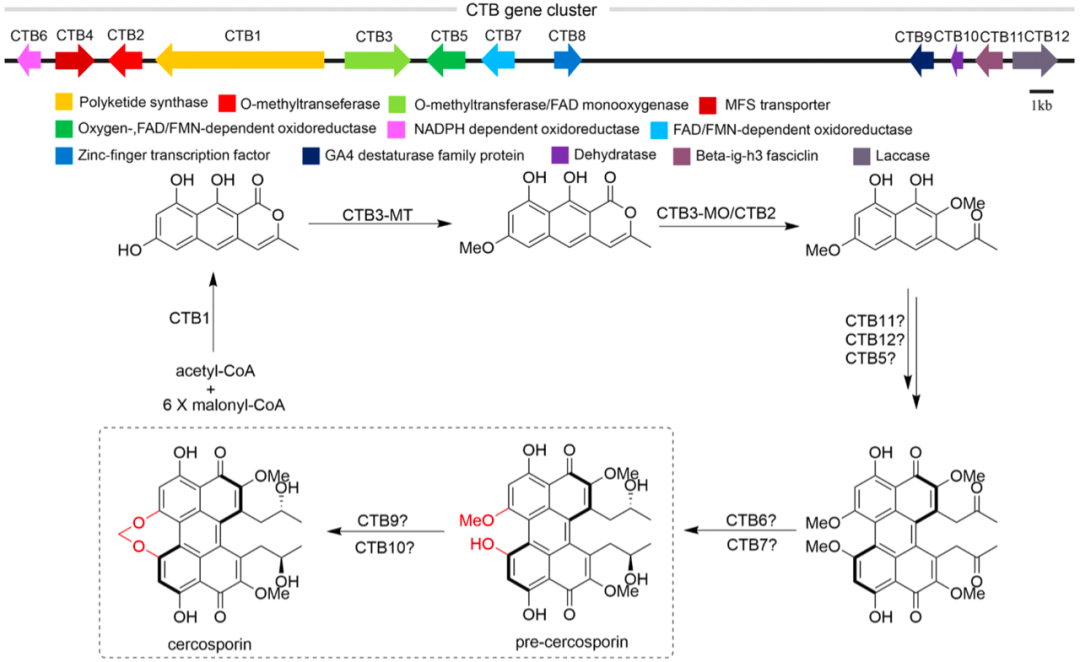
Figure 1. The biosynthetic gene cluster of cercosporin and their proposed biosynthetic pathway.
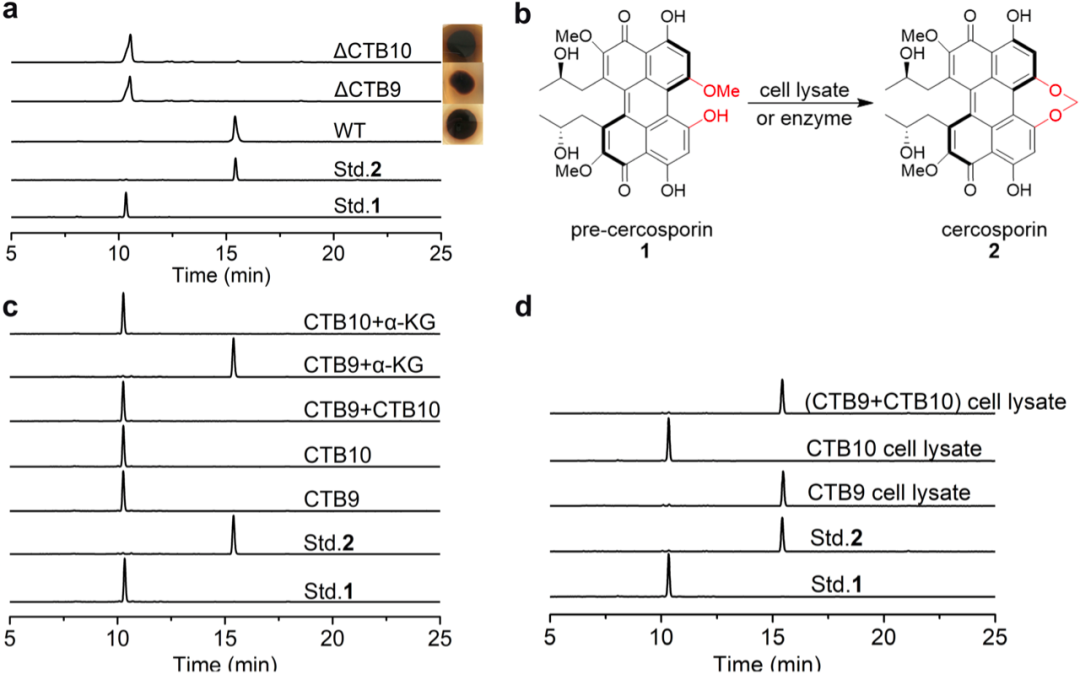
Figure 2. In vitro enzymatic conversion of pre-cercosporin 1 to cercosporin 2 catalyzed by CTB9 and CTB10.
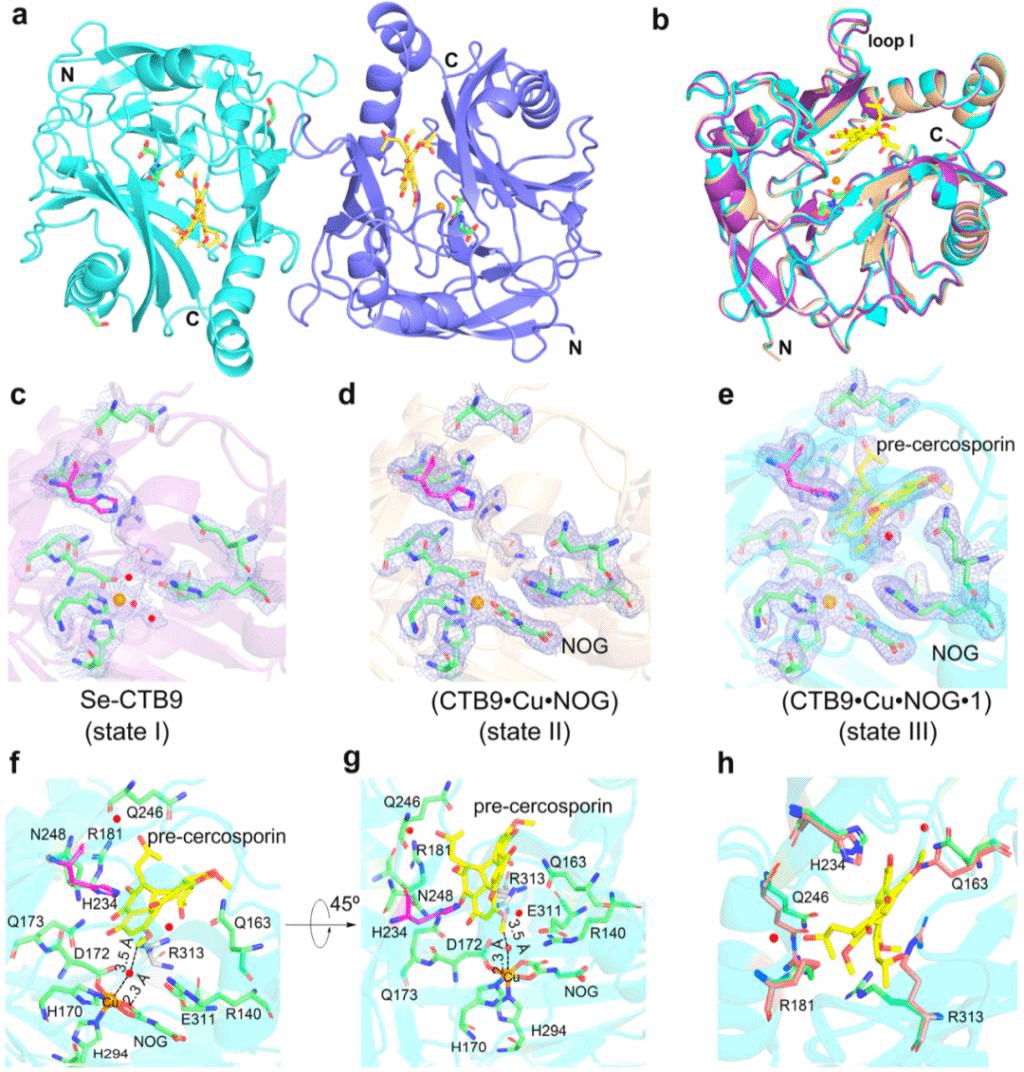
Figure 3. Crystal structures of Se-CTB9 (7EUS), CTB9•Cu•NOG (7EUT) and CTB9•Cu•NOG•1 (7EUU).
此外,基于以往五元或六元亚甲基二氧桥环的形成机理和有关Fe(II)/α-KG依赖加氧酶催化反应的报道,作者提出了两条合理的催化机制来揭示尾孢菌素中七元亚甲基二氧桥环的形成过程(Fig. 4)。途径1中,Fe(IV)=O基团从pre-cercosporin反应位点的甲氧基上攫取一个氢原子,形成Fe(III)-OH络合物F和pre-cercosporin碳自由基。经过氧回弹后,与一个水分子形成Fe(II)-H2O络合物G,最后pre-cercosporin反应位点上的羟甲基脱水后转化为佯盐H,并通过分子内亲核加成反应形成cercosporin。而在途径2中,Fe(IV)=O基团从pre-cercosporin酚羟基上攫取的一个氢原子,形成Fe(III)-OH络合物I和pre-cercosporin氧自由基。随后,配合物I经过质子转移和电子转移,生成配合物J,然后形成亚甲基二氧桥环,得到cercosporin。
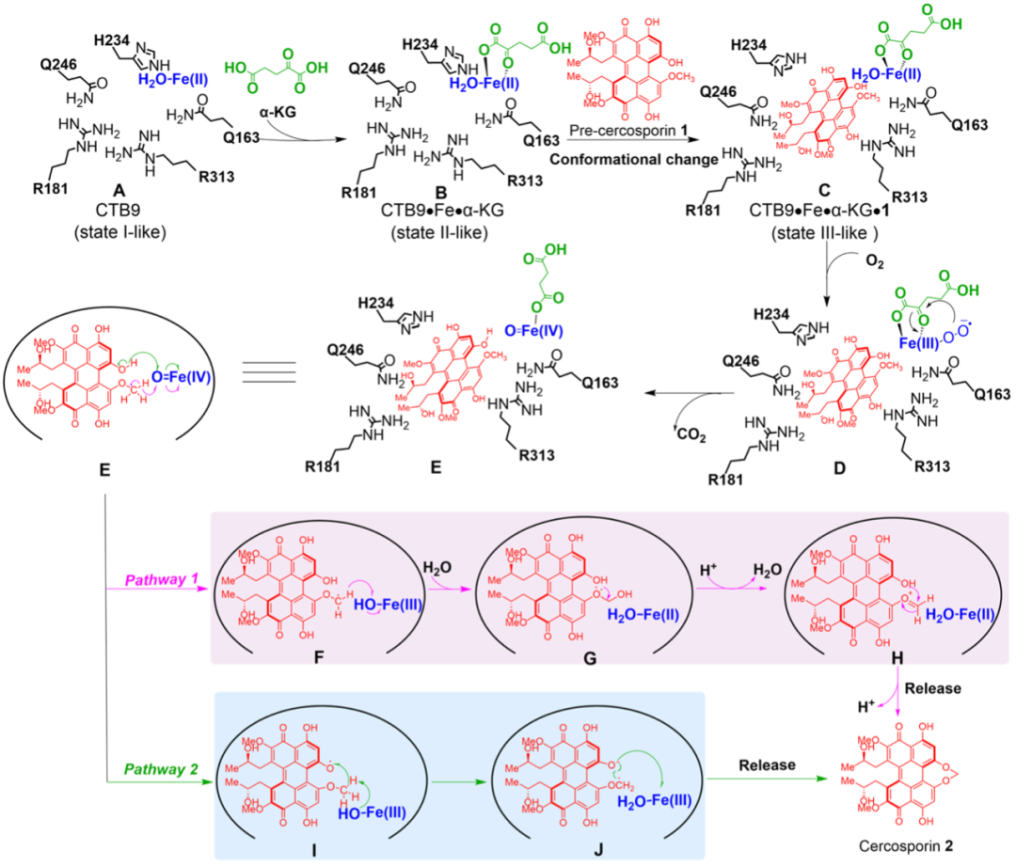
Figure 4. Proposed mechanism of seven-membered MDB formation catalyzed by CTB9.
为了进一步确定CTB9的详细反应机理,作者进行了量子化学计算。首先,基于蛋白复合物晶体结构和几何优化后得到了三种酶-底物复合物的活性位点模型(Model A, Model B, Model C)。随后,作者选择能量最低的Model B对CTB9催化生成七元亚甲基二氧桥环的过程进行量子化学计算(Fig. 5a)。结果表明,从酚羟基上攫取氢原子实际上是一个质子转移介导的电子转移过程,避免了较大的O-H键解离能,从而使其能垒比从甲氧基上攫取氢原子要低得多,最终确定了CTB9经过途径2催化pre-cercosporin形成天然产物cercosporin更为合理(Fig. 5b)。
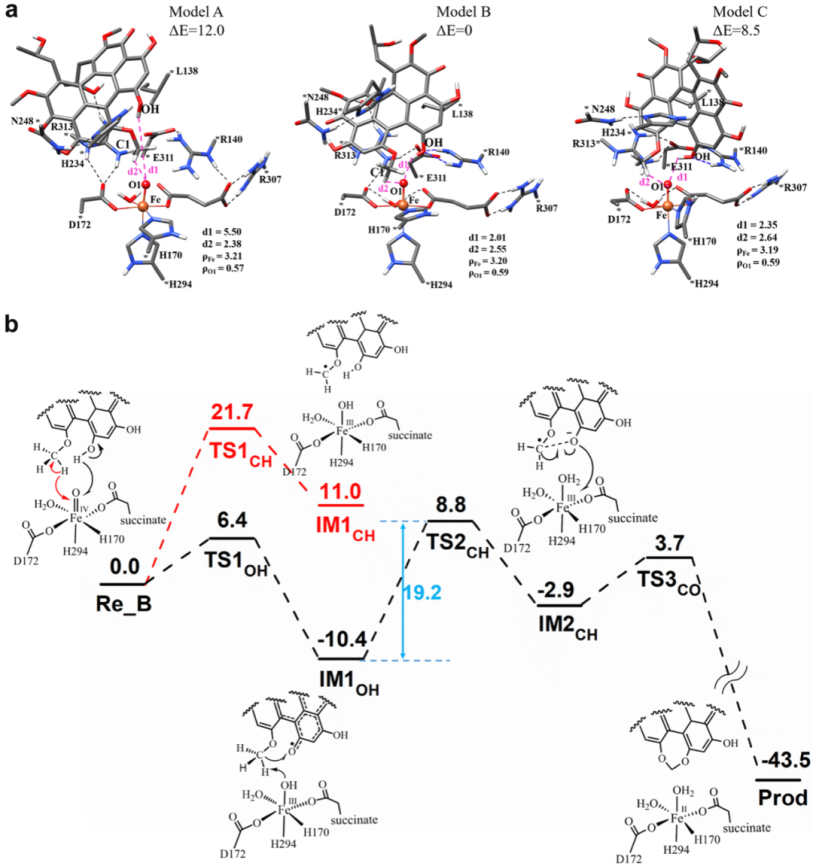
Figure 5. Quantum mechanical investigation of seven-membered MDB formation catalyzed by CTB9.
上述工作在线发表在ACS Catalysis (https://doi.org/10.1021/acscatal.1c04627),江南大学糖化学与生物技术教育部重点实验室硕士生刘旋忠、袁振波助理研究员、博士生侯晓冬、中国科学院天津工业生物技术研究所的苏浩为该论文的共同第一作者,饶义剑教授和中国科学院天津工业生物技术研究所的盛翔教授为该论文的共同通讯作者。上述研究工作得到了国家重点研发计划(2018YFA0901700)和江苏省自然科学基金(BK20202002)等基金资助。
